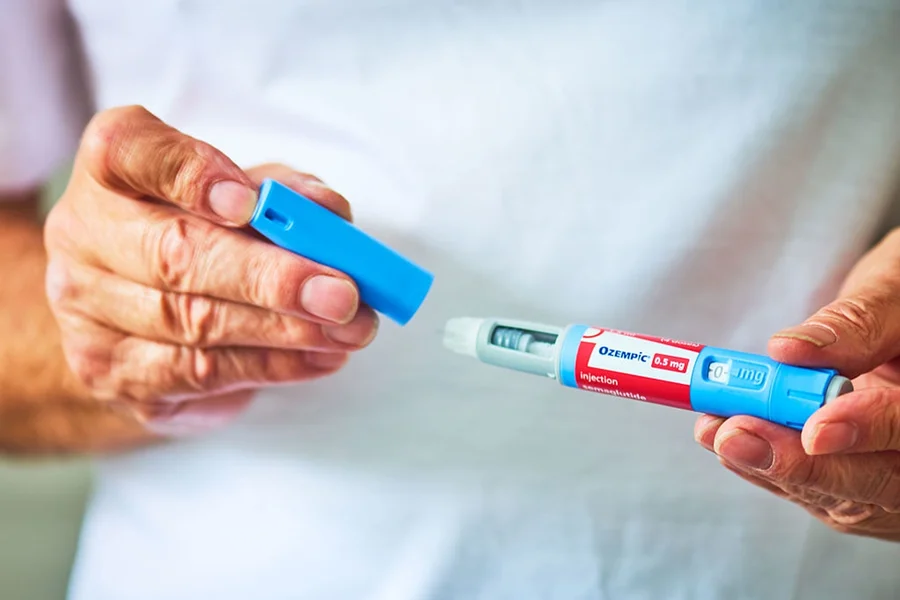
A Agência Nacional de Vigilância Sanitária (Anvisa) está analisando atualmente 17 pedidos relacionados a medicamentos com o princípio ativo semaglutida, substância utilizada no tratamento de diabetes tipo 2 e também associada ao controle de peso. O movimento ocorre após o vencimento da patente no Brasil, registrado na última sexta-feira (20/03).
Segundo levantamento da própria agência, oito processos já estão em análise, enquanto outros nove ainda aguardam o início da avaliação técnica. Entre os pedidos analisados, sete são de origem sintética e um de origem biológica.
Apesar do fim da patente, a comercialização de novos medicamentos no país depende obrigatoriamente do registro sanitário, que exige a comprovação de eficácia, segurança e qualidade. A maior parte das solicitações chegou à Anvisa ao longo de 2025, após a publicação de um edital que priorizou a análise de medicamentos análogos ao GLP-1, classe à qual pertence a semaglutida.
Atualmente, dois pedidos de medicamentos sintéticos estão em fase de exigência técnica, ou seja, dependem do envio de informações complementares pelas empresas responsáveis. Já os demais processos devem receber parecer preliminar até o fim de abril, podendo resultar em aprovação, reprovação ou novas exigências.
Além disso, a Anvisa destaca que a avaliação desse tipo de medicamento é considerada um desafio técnico em nível global. Até o momento, nenhuma grande agência reguladora internacional aprovou versões sintéticas da semaglutida.
A complexidade está relacionada às características desses produtos, que combinam aspectos de medicamentos sintéticos e biológicos. Isso exige análises rigorosas, incluindo estudos sobre impurezas, imunogenicidade e estabilidade, para garantir que não causem reações adversas ou perda de eficácia nos pacientes.
A iniciativa faz parte de um esforço para ampliar o acesso a tratamentos no país, mantendo os padrões de segurança sanitária exigidos pela legislação brasileira.